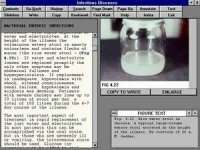
Антиковидный препарат AstraZeneca снижает риск заражения на 77% в течение полугода
По итогам первичного анализа данных клинического исследования III фазы TACKLE, в ходе которого оценивалась эффективность препарата на основе моноклональных антител для доконтактной профилактики COVID-19, было показано, что препарат снижает риск развития симптомов коронавирусной инфекции на 77% по сравнению с плацебо.
В свою очередь расширенный анализ данных при медиане наблюдения 196 дней продемонстрировал снижение риска развития симптомов COVID-19 на 83% в группе контроля. Симптомы COVID-19 развились у 11 из 3441 добровольцев (0,3%) из контрольной группы и у 31 из 1731 (1,8%) из группы плацебо.
В группе контроля по итогам наблюдения за шесть месяцев не было зафиксировано случаев тяжелого течения COVID-19 и летальных исходов. В группе плацебо было зафиксировано пять случаев тяжелого течения заболевания, семь случаев госпитализаций и два летальных исхода.
Препарат продемонстрировал хороший профиль безопасности и переносимости. Наиболее распространенным нежелательным явлением стала реакция в месте инъекции, развившаяся у 2,4% участников группы контроля и у 2,1% участников группы плацебо.
Данные дополнительного анализа фармакокинетики препарата показали, что его концентрация в сыворотке крови сохранялась в течение шести месяцев после введения, что подтверждает обеспечение долгосрочной защиты от COVID-19.
Препарат на основе моноклональных антител AZD7442 представляет собой комбинацию из двух антител длительного действия — тиксагевимаба (AZD8895) и цилгавимаба (AZD1061), полученных из B-клеток реконвалесцентов SARS-CoV-2 (severe acute respiratory syndrome coronavirus 2 — тяжелый острый респираторный синдром, вызванный коронавирусом 2-го типа). Препарат был одобрен к применению для доконтактной профилактики COVID-19 в США, Европейском Союзе, Великобритании и ряде других стран.
По итогам первичного анализа данных клинического исследования III фазы TACKLE, в ходе которого оценивалась эффективность препарата на основе моноклональных антител для доконтактной профилактики COVID-19, было показано, что препарат снижает риск развития симптомов коронавирусной инфекции на 77% по сравнению с плацебо.
В свою очередь расширенный анализ данных при медиане наблюдения 196 дней продемонстрировал снижение риска развития симптомов COVID-19 на 83% в группе контроля. Симптомы COVID-19 развились у 11 из 3441 добровольцев (0,3%) из контрольной группы и у 31 из 1731 (1,8%) из группы плацебо.
В группе контроля по итогам наблюдения за шесть месяцев не было зафиксировано случаев тяжелого течения COVID-19 и летальных исходов. В группе плацебо было зафиксировано пять случаев тяжелого течения заболевания, семь случаев госпитализаций и два летальных исхода.
Препарат продемонстрировал хороший профиль безопасности и переносимости. Наиболее распространенным нежелательным явлением стала реакция в месте инъекции, развившаяся у 2,4% участников группы контроля и у 2,1% участников группы плацебо.
Данные дополнительного анализа фармакокинетики препарата показали, что его концентрация в сыворотке крови сохранялась в течение шести месяцев после введения, что подтверждает обеспечение долгосрочной защиты от COVID-19.
Препарат на основе моноклональных антител AZD7442 представляет собой комбинацию из двух антител длительного действия — тиксагевимаба (AZD8895) и цилгавимаба (AZD1061), полученных из B-клеток реконвалесцентов SARS-CoV-2 (severe acute respiratory syndrome coronavirus 2 — тяжелый острый респираторный синдром, вызванный коронавирусом 2-го типа). Препарат был одобрен к применению для доконтактной профилактики COVID-19 в США, Европейском Союзе, Великобритании и ряде других стран.